2015년03월11일 3번
[과목 구분 없음] 다음은 산 염기 반응의 화학 반응식이다.
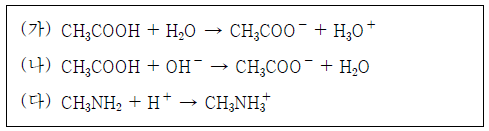
이에 대한 옳은 설명만을 <보기>에서 있는 대로 고른 것은?
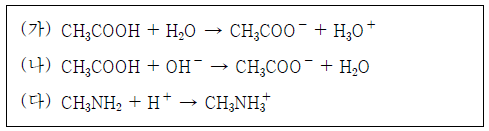
이에 대한 옳은 설명만을 <보기>에서 있는 대로 고른 것은?

- ① ㄱ
- ② ㄴ
- ③ ㄱ, ㄷ
- ④ ㄴ, ㄷ
- ⑤ ㄱ, ㄴ, ㄷ
(정답률: 알수없음)
문제 해설
- 보기에서 정답이 "ㄱ"인 이유: 이 반응은 산과 염기가 중화되는 반응이므로, 생성물인 물과 염이 이온으로 존재하게 된다. 이온은 전기적으로 중성이므로, 반응식에서 이온의 수가 같아야 한다. 따라서, H+ 이온과 OH- 이온의 수가 같은 H2O로 중화되는 것이 옳다.
- 보기에서 정답이 "ㄴ"인 이유: 반응식에서 Na+ 이온과 Cl- 이온이 생성되는 것을 볼 수 있다. 이는 NaOH와 HCl가 중화되어 생성되는 것으로, NaCl은 중화 염이다.
- 보기에서 정답이 "ㄱ, ㄷ"인 이유: 반응식에서 H+ 이온과 OH- 이온이 결합하여 H2O가 생성되는 것은 "ㄱ"에서 설명한 대로이다. 또한, Na+ 이온과 Cl- 이온이 결합하여 NaCl이 생성되는 것은 "ㄴ"에서 설명한 대로이다. 따라서, "ㄱ"과 "ㄴ" 모두 맞는 것이다.
- 보기에서 정답이 "ㄴ, ㄷ"인 이유: 반응식에서 H+ 이온과 OH- 이온이 결합하여 H2O가 생성되는 것은 "ㄱ"에서 설명한 대로이다. 하지만, 반응식에서 Na+ 이온과 Cl- 이온이 결합하여 NaOH가 생성되는 것은 옳지 않다. NaOH는 염기이므로, HCl과 중화되어 NaCl이 생성되어야 한다. 따라서, "ㄴ"은 맞지만 "ㄷ"는 틀린 것이다.
- 보기에서 정답이 "ㄱ, ㄴ, ㄷ"인 이유: "ㄱ"에서는 H+ 이온과 OH- 이온이 결합하여 H2O가 생성되는 것을 설명하였다. "ㄴ"에서는 NaOH와 HCl가 중화되어 NaCl이 생성되는 것을 설명하였다. "ㄷ"에서는 HCl과 NaOH가 결합하여 NaCl과 H2O가 생성되는 것을 설명하였다. 따라서, 모두 맞는 것이다.
- 보기에서 정답이 "ㄴ"인 이유: 반응식에서 Na+ 이온과 Cl- 이온이 생성되는 것을 볼 수 있다. 이는 NaOH와 HCl가 중화되어 생성되는 것으로, NaCl은 중화 염이다.
- 보기에서 정답이 "ㄱ, ㄷ"인 이유: 반응식에서 H+ 이온과 OH- 이온이 결합하여 H2O가 생성되는 것은 "ㄱ"에서 설명한 대로이다. 또한, Na+ 이온과 Cl- 이온이 결합하여 NaCl이 생성되는 것은 "ㄴ"에서 설명한 대로이다. 따라서, "ㄱ"과 "ㄴ" 모두 맞는 것이다.
- 보기에서 정답이 "ㄴ, ㄷ"인 이유: 반응식에서 H+ 이온과 OH- 이온이 결합하여 H2O가 생성되는 것은 "ㄱ"에서 설명한 대로이다. 하지만, 반응식에서 Na+ 이온과 Cl- 이온이 결합하여 NaOH가 생성되는 것은 옳지 않다. NaOH는 염기이므로, HCl과 중화되어 NaCl이 생성되어야 한다. 따라서, "ㄴ"은 맞지만 "ㄷ"는 틀린 것이다.
- 보기에서 정답이 "ㄱ, ㄴ, ㄷ"인 이유: "ㄱ"에서는 H+ 이온과 OH- 이온이 결합하여 H2O가 생성되는 것을 설명하였다. "ㄴ"에서는 NaOH와 HCl가 중화되어 NaCl이 생성되는 것을 설명하였다. "ㄷ"에서는 HCl과 NaOH가 결합하여 NaCl과 H2O가 생성되는 것을 설명하였다. 따라서, 모두 맞는 것이다.
연도별
- 2016년09월01일
- 2016년07월06일
- 2016년06월02일
- 2016년04월06일
- 2016년03월10일
- 2015년11월12일
- 2015년10월13일
- 2015년09월02일
- 2015년07월09일
- 2015년06월04일
- 2015년04월09일
- 2015년03월11일
- 2014년11월13일
- 2014년10월07일
- 2014년09월03일
- 2014년07월10일
- 2014년06월12일
- 2014년04월10일
- 2014년03월12일
- 2013년11월07일
- 2013년10월08일
- 2013년09월03일
- 2013년07월12일
- 2013년06월05일
- 2013년04월11일
- 2013년03월13일
- 2012년11월08일
- 2012년10월09일
- 2012년09월04일
- 2012년07월11일
- 2012년06월07일
- 2012년04월10일
- 2011년10월12일
- 2011년09월01일
- 2011년07월13일
- 2011년06월02일
- 2011년04월12일
- 2011년02월28일
- 2010년11월18일
- 2010년10월12일
- 2010년09월02일
- 2010년07월08일
- 2010년06월10일
- 2010년04월13일
- 2010년03월12일
- 2009년11월12일
- 2009년10월15일
- 2009년09월03일
- 2009년07월14일
- 2009년06월04일
- 2009년04월15일
- 2009년03월13일
- 2008년11월13일
- 2008년10월16일
- 2008년09월04일
- 2008년07월15일
- 2008년06월04일
- 2008년04월15일
- 2008년03월14일
- 2007년11월15일
- 2007년10월10일
- 2007년09월06일
- 2007년07월12일
- 2007년06월07일
- 2007년03월16일
- 2006년11월16일
- 2006년10월12일
- 2006년09월06일
- 2006년06월03일
- 2006년04월19일
- 2006년03월11일

